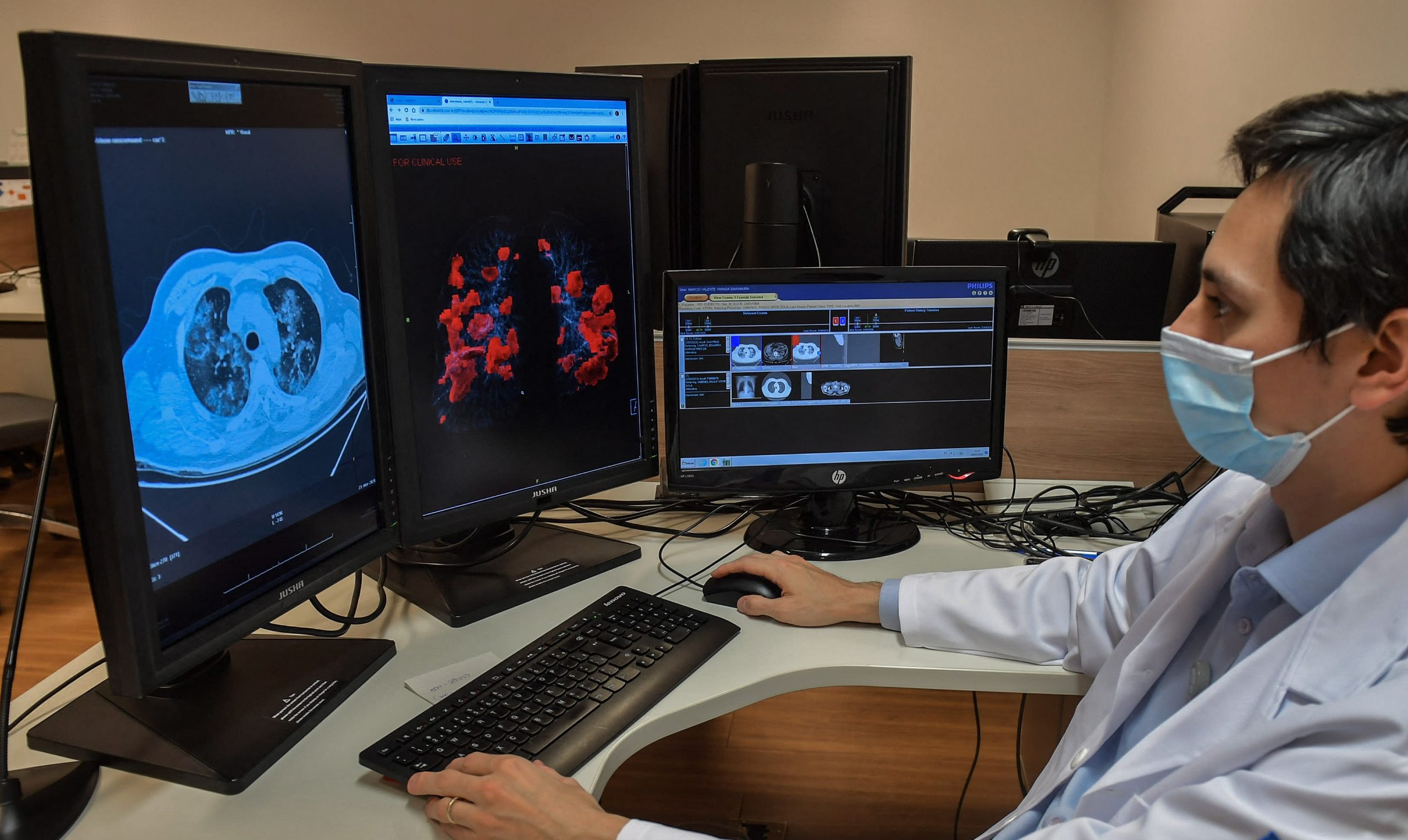
Was in vielen Labors und Kliniken schon Alltag ist
Intelligente Algorithmen werden zu Experten in wichtigen medizinischen Fragestellungen trainiert - und das naturgemäß ohne Anzeichen von Frust oder Ermüdung: Die Palette reicht dabei von Sepsis über Demenz bis zu Krebs. Nachfolgend ein Streifzug durch heimische Labors und Kliniken.

Risiko für Alzheimerkrankheit bestimmen
Die Früherkennung der Alzheimerkrankheit ist wichtig, um rechtzeitig mit einem geeigneten Lebensstil und medikamentöser Behandlung einem raschen Verfall der kognitiven Kapazitäten entgegenzuwirken, erklären Lucas Paletta und Silvia Russegger von Joanneum Research in Graz: „Ohne KI gibt es in den Analysetechnologien keine Möglichkeit, subtile Zusammenhänge in multimodalen Daten festzustellen, die notwendig sind, um möglichst frühzeitig Abweichungen von gesunden Merkmalsprofilen festzustellen.“ Im Projekt PREDICTOM, das soeben begonnen hat, entwickelt man ein „Ernsthaftes Spiel“ (Serious Game), bei dem das Blickverhalten der Probandinnen und Probanden beobachtet wird, denn gewisse charakteristische Blickmerkmale ermöglichen eine frühe Identifikation eines erhöhten Demenzrisikos.
Durchführen könnte man solche Tests in der Praxis niedergelassener Ärzte. „Dabei werden der Patientin oder dem Patienten schrittweise Aufgaben gestellt, die zur Lösung die kognitive Kontrolle des Blickverhaltens erfordern“, so Paletta: „Die KI gewichtet dann verschiedenste Merkmale des Blickverhaltens und generiert automatisch einen entsprechenden Bericht für die Ärztinnen und Ärzte als Grundlage zur Entscheidungsfindung.“ Der Test soll in maximal 30 Minuten durchführbar sein, um möglichst viele Verdachtsfälle abdecken zu können.
Knochenfehlstellungen routiniert erkennen
„Trotz großer technischer Fortschritte werden Röntgenbilder im klinischen Alltag weiterhin von Ärztinnen und Ärzten manuell beurteilt, vermessen und narrativ beschrieben“, erklärt Stefan Nehrer vom Zentrum für Regenerative Medizin der Universität für Weiterbildung Krems. Dabei schleichen sich durch Stress, Ermüdung und Unachtsamkeiten manchmal Fehler ein, laut Studien werden vier bis dreißig Prozent der Röntgenbilder nicht optimal diagnostiziert. Intelligente Software soll den menschlichen Befundern helfen, Fehler zu vermeiden.
Im Forschungsprojekt Künstliche Intelligenz in der orthopädischen Röntgendiagnostik, arbeitete Nehrer zusammen mit der Wiener Firma ImageBiopsy Lab daran, KI-Modelle in den Routinebetrieb zu integrieren, zum Beispiel um Knie-Arthorose-Grade exakt festzustellen, Hüften automatisch zu vermessen, ebenso Beinachsen. Solche Messungen sollten möglichst standardisiert und reproduzierbar sein, was mithilfe von Computeralgorithmen gut zu bewerkstelligen ist. „Das verringert die Arbeitslast der Experten und verbessert die Qualität der Diagnosen“, meint Nehrer. Das Projekt sei schon seit 2022 klinisch implementiert: „Wichtig dafür war eine einfache Usability (Benutzbarkeit, Anm.), die Anwendung mit KI darf nicht komplizierter sein, also ohne KI“, so der Experte.


Algorithmus schlägt Medikation gegen Blutstrominfektion vor
Ein KI-System, das Clemens Heitzinger von der Fakultät für Informatik und dem Center for Artificial Intelligence and Machine Learning (CAIML) der Technischen Universität (TU) Wien mit seinem Team verwirklichte, schlägt bei Sepsis-Patientinnen und -Patienten (Personen mit einer Infektion des Blutstroms, oft Blutvergiftung genannt) die beste Medikation vor. „Es kann auf Intensivstationen routinemäßig eingesetzt werden“, sagt er. Sepsis sei dort die häufigste Erkrankung und als multifaktorielle Erkrankung schwierig zu diagnostizieren sowie zu behandeln.
„Wir haben Algorithmen des „bestärkenden Lernens“ (reinforcement learning) entwickelt, die aus historischen Aufzeichnungen von Zehntausenden Patienten die bestmöglichen Behandlungsstrategien berechnen“, berichtet er: „Unser KI-System stellt damit den behandelnden Ärztinnen und Ärzten jahrzehntelange Erfahrung in kürzester Zeit zur Verfügung.“ Die Behandlungsstrategien sind sogar individuell auf die Person zugeschnitten, da sie immer an den aktuellen Zustand einer Patientin oder eines Patienten angepasst sind. „Das Prinzip ist auf jede Krankheit anwendbar, für die ausreichende historische Datensammlungen zur Verfügung stehen“, erklärt Heitzinger.
Knochenbrüche in Röntgenbildern diagnostizieren
Manche subtilen Brüche sind schwer auf Röntgenbildern zu sehen. KI-Algorithmen sollen Unfallchirurginnen und Radiologen helfen, indem sie wie eine ärztliche Zweitmeinung einen zusätzlichen Befundvorschlag machen und mögliche Frakturen markieren. „Vor allem jungen Ärztinnen und Ärzten kann so bei der Diagnosestellung geholfen werden“, berichtet Rosmarie Breu, die am Ludwig Boltzmann Institut für Traumatologie in Wien mit der Wiener Firma ImageBiopsy Lab eine Software entwickelte, die Handgelenkbrüche erkennt. Bis dato wird bei den Patienten manchmal das betroffenen Gelenk prophylaktisch ruhig gestellt, wenn ein Bruch weder eindeutig feststellbar noch auszuschließen ist. Es folgen vor allem aber weitere Kontrollen (mit zusätzlichen Röntgenuntersuchungen, die jeweils eine Strahlenbelastung bringen), Unsicherheiten, und teils kostenaufwändige Computertomographie-Aufnahmen.
„Ich habe die Brüche auf den Röntgenbildern für das Softwaretraining markiert, um der Software vor allem anfangs beizubringen, wie ein Bruch ausschaut“, erklärt Breu: „Nach und nach lernte sie dann durch große Datenmengen dazu.“ „Für die durchgeführte Studie wurde die KI mit mehr als 20.000 Bildern trainiert“, berichtet Richard Ljuhar von ImageBiopsy Lab. In Zukunft will man die Software trainieren, „an jedem Knochen des menschlichen Körpers einen Bruch verlässlich zu erkennen“, so Breu: „Die künstliche Intelligenz soll bei schwer sichtbaren Brüchen eine Hilfe bieten, aber auch beim Vorliegen mehrerer Brüche verhindern, dass man zunächst nur den offensichtlichen Bruch erkennt und eventuell eine weitere Fraktur übersieht.“


Dem Demenzrisiko auf der Spur
Im EU-Projekt LETHE soll bei Personen vor allem mittleren Alters ein Demenzrisiko mittels KI frühzeitig erkannt werden, nämlich bevor sie Patientinnen oder Patienten sind, erklärt Sten Hanke vom eHealth Institute an der Fachhochschule (FH) Joanneum in Graz. Die dort entwickelte KI könne auch im klinischen Alltag eingesetzt werden, um zu beurteilen, wie die Therapie von Patienten bestmöglich weitergeführt wird. „KI-Methoden bieten die Möglichkeit, eine Vielzahl von digital erhobenen ‚Biomarkern‘ zu analysieren“, sagt er: „Bei dem Projekt sind das vor allem Informationen bezüglich des Lebensstils der Personen, zum Beispiel, über die Ernährung und Bewegung.“ Ziel ist es, klare Zusammenhänge zwischen diesen Biomarkern und dem Demenzrisiko zu erkennen.
Derzeit läuft in dem Projekt eine Interventionsstudie mit etwa 160 Teilnehmerinnen und Teilnehmern in vier europäischen Ländern. „Es werden sowohl klinische als auch digitale Daten gesammelt, und die Probandinnen erhalten per App vielfältige Unterstützung in Bezug etwa auf ihre tägliche Aktivität, Ernährung und kognitives Training.“ Das Ziel wäre eine genaue Risikobeurteilung bezüglich Demenz, sowie individualisierte Maßnahmen zu empfehlen, diesem Risiko entgegenzuwirken, oder die Person in eine geeignete Therapie zu überführen. „Das Dashboard mit der Risikobeurteilung kann auch beim niedergelassenen Neurologen, Hausarzt sowie in der klinischen Aufnahme Verwendung finden“, so der Experte.
Diabetestherapie bei Kindern verbessern
Mit KI lässt sich das Management von Diabetes Typ I bei Kindern und Kleinkindern verbessern, sagt Sabine Hofer von der Universitätsklinik für Pädiatrie I der Medizinischen Universität Innsbruck. Ein intelligenter Algorithmus steuert dabei eine Insulinpumpe je nach dem Blutzuckergehalt, den ein Glukosesensor, den die Kinder tragen, anzeigt. Er ist als CamAPS FX App am Handy der Youngsters gespeichert. „Die Glukosewerte im Zielbereich von 70 bis 180 Milligramm pro Deziliter zu halten ist mit jeder Insulintherapie eine große Herausforderung“, erklärt sie: „Durch die mögliche Feindosierung der Insulinzufuhr durch die KI werden die Glukosewerte genauer und längere Zeit im Zielbereich gehalten.“
Das von der EU geförderte Projekt Kids-AP wurde in England, Deutschland, Luxemburg und Österreich bei Kleinkindern unter sieben Jahren durchgeführt. „Das System konnte auch in der sehr jungen Altersgruppe sicher und effektiv angewandt werden“, so Hofer. Die Studie ist abgeschlossen, und der Algorithmus ist „kommerziell erhältlich und allen Menschgen mit Typ 1 Diabetes zugänglich“, erklärt sie.


Tumordiagnose während Gehirn-OP
Künstliche Intelligenz ist in der Lage, Tumorgewebe im Zentralnervensystem (Gehirn und Rückenmark) während einer Operation zu analysieren, berichtet Georg Widhalm von der Onkologischen Ambulanz an der Universitätsklinik für Neurochirurgie von MedUni Wien und AKH Wien. Zur besseren Einschätzung der Tumorart wird häufig eine solche Gewebeanalyse durchgeführt. Bis die Ergebnisse vorliegen, dauert es mit der konventionellen neuropathologischen Schnellschnitt-Befundung im internationalen Schnitt ungefähr eine halbe Stunde, währenddessen die Patientinnen und Patienten in Narkose bleiben müssen. „Dies ist vor allem durch den Transport des Materials sowie die aufwendige Anfertigung der Gewebeschnitte bedingt“, erklärt der Mediziner: „Mit einem neuartigen Gerät kann aber ein hochauflösendes, digitales Bild vom Gewebe innerhalb weniger Minuten direkt im Operationssaal erstellt werden, das sofort von Neuropathologen virtuell aufgerufen und befundet werden kann.“
Zusätzlich werden mithilfe von KI rasche automatisierte Analysen durchgeführt, welche mit hoher Wahrscheinlichkeit schon während der OP innerhalb weniger Minuten verschiedene Tumormerkmale voraussagen. „In der Anfangszeit konnten nur häufig vorkommende Tumorarten bestimmt werden, durch Sammlung größerer Datenmengen werden zukünftig auch immer seltenere Tumorarten besser erkannt werden“, sagt Widhalm. Man erhält nicht nur Informationen über die Tumorart und (molekulare) Subtypen, sondern mittels einer neuen KI kann das Gewebe auch auf das Vorliegen von Resttumorgewebe analysiert werden. Chirurginnen und Chirurgen können mit dem Gerät mehrfache Randproben überprüfen, was konventionell viel zu zeitaufwendig wäre. „Diese KI erleichtert dadurch die Detektion der Tumorgrenze, die oft sehr schwer erkennbar ist“, erklärt er. Damit wäre ein wichtiges Ziel besser erreichbar: eine maximal sichere Tumorentfernung. Es besteht dadurch die Hoffnung, dass zukünftig sehr belastende, frühe Zweiteingriffe damit vermieden werden können oder ihre Zahl deutlich reduziert wird. „Der erfolgreiche Einsatz dieser neuen Technik ist das Ergebnis der engen Zusammenarbeit mehrerer Universitätskliniken im Rahmen des an MedUni Wien und AKH Wien neu etablierten Comprehensive Centers for Clinical Neurosciences and Mental Health„, so Widhalm.
Epilepsiediagnose bei Kindern und Jugendlichen
Die Diagnose von Epilepsie ist für Medizinerinnen und Mediziner enorm zeitaufwendig, sagt Malgorzata Wislowska von der Forschungsabteilung Medical Signal Analysis am Austrian Institute of Technology (AIT) in Wien. Um abnormale Hirnaktivität zu erkennen, erfolgt bei Patientinnen und Patienten eine kontinuierliche EEG-Aufzeichnung (Elektroenzephalogramm) über mehrere Tage. „In der herkömmlichen Vorgehensweise erkennt danach ein Spezialist anhand visueller Inspektion im Gehirnsignal wichtige Muster wie epileptische Anfälle oder epileptische Spikes“, so Wislowska: „In der klinischen Praxis müssen bei 24-stündigen Aufzeichnungen 5.760 Bildschirmseiten EEG-Kurven durchgesehen werden.“ Es gäbe auch nur eine „begrenzte Anzahl von Spezialistinnen und Spezialisten mit entsprechender Ausbildung und ausreichender Erfahrung, um die EEG-Signale zuverlässig zu interpretieren.“
Im Projekt EpiCare4Kids wird eine KI-Anwendung entwickelt, die EEGs von Kindern und Jugendlichen analysieren und Auffälligkeiten kennzeichnen soll. Es gibt zwar schon einen Algorithmus für die Untersuchung von erwachsenen Patienten mit Epilepsie, der in der Analysesoftware encevis eingebaut ist. „Die gesunde und pathologische Gehirnaktivität von Kindern unterscheidet sich aber erheblich von der von Erwachsenen“, sagt Wislowska. Deshalb müsse man die Künstliche Intelligenz mit Daten von Kindern trainieren. Die fertige Software soll vollständig automatisiert auffällige Gehirnmuster im EEG-Signal erkennen und die Neurologinnen und Neurologen darauf hinweisen, erklärt sie: „So kann schnell eine präzise Diagnose erstellt und eine geeignete Behandlung gewählt werden.“


Hautkrebsdiagnose mit KI
Maschinelles Lernen soll Medizinerinnen und Mediziner bei der Diagnose von Hautkrebs unterstützen. Zum Einen können mithilfe von KI verdächtige Hautstellen untersucht werden, bei denen nicht klar ist, ob man sie entfernen soll, oder nicht, so Harald Kittler von der Universitätsklinik für Dermatologie der Medizinischen Universität (Meduni) Wien: Auch bei Patientinnen und Patienten mit vielen Muttermalen sei die speziell trainierte Künstliche Intelligenz einsetzbar. Sie soll vorwiegend Ärztinnen und Ärzte unterstützen, die keine große Erfahrung in der Diagnose von Hautkrebs haben, damit sie dies auf Expertenniveau bewerkstelligen.
„Zunächst konstruierten wir eine KI für die Diagnose von pigmentierten Hautläsionen“, berichtet Kittler: „Wahrscheinlich viel wichtiger ist aber, dass wir Forschungsgruppen auf der ganzen Welt (anonymisiertes) Bildmaterial zur Verfügung stellten, damit sie ihre eigenen KI-Anwendungen trainieren und testen können.“ Anschließende Tests zeigten, dass diese Anwendungen menschlichen Expertinnen und Experten bei der Hautkrebsdiagnose durchaus ebenbürtig sind.
„Ziel ist, dass wir Gesundheitspersonal mit einer KI ausrüsten, um die Diagnose zu verbessern“, erklärt er. Zum Beispiel, ob man Patienten zu Spezialisten weiterschicken soll, oder eine Hautveränderung als unbedenklich einzustufen ist. „Die Therapieentscheidung bleibt aber immer den menschlichen Diagnostikern vorbehalten“, sagt der Experte. Dazu gehört auch die Entscheidung, ob man den Ratschlag der Künstlichen Intelligenz berücksichtigen oder verwerfen soll. Außerdem gibt es bei vielen Patientinnen und Patienten Begleitumstände, die Therapieentscheidungen wesentlich beeinflussen. „Diese kennt freilich nur der Arzt und kann sie berücksichtigen, nicht aber die KI-Anwendungen“, so Kittler.
Verbesserte Hirntumordiagnostik und -behandlung
Künstliche Intelligenz hilft im von Isabell Ganitzer von RISC Software (Hagenberg, ÖO) geleiteten Projekt nARvibrain dabei, medizinische Bild- und Testdaten sowie Simulationsergebnisse von Gehirntumor-Patienten zu verarbeiten und daraus eine umfassende digitale Darstellung der betroffenen Person zu generieren.
Die KI unterstützt zudem bei Untersuchungen mittels transkranieller Magnetstimulation (TMS) vor einer Operation zur Tumorentfernung. Die Software macht (basierend auf dem Modell, das sie zuvor von der Person erstellt hat) einen Vorschlag zur optimalen Ausrichtung und Positionierung der dafür nötigen TMS-Spule. So werden wichtige Gehirnbereiche etwa für die Sprache und Bewegung ermittelt, sodass diese bei einer Tumorentfernung im Hirn des Patienten optimal geschont werden. „Darüber hinaus werden neuartige Magnetresonanztomographie (MRT)-Verfahren zur verbesserten Darstellung der Nervenfaserbahnen und neuartige Stimulationsverfahren zur Abbildung von funktionellen Gehirnaktivitäten entwickelt“, so Ganitzer.
In dem von der österreichischen Forschungsförderungsgesellschaft (FFG) geförderten Projekt, das RISC Software gemeinsam mit dem Linzer Technologie-Start-up cortEXplore, der Fachhochschule (FH) Joanneum (Graz) und der Medizinischen Universität Graz durchführt, werden zudem 3D-Visualisierungsmöglichkeiten geschaffen, damit Medizinerinnen und Mediziner den Patienten ihren Krankheitszustand und den geplanten Behandlungsablauf anschaulicher erklären können. Die entwickelte Technologie soll zusätzlich für eine Didaktik-Plattform für Medizin-Studierende verwendet werden, um neuro-anatomische Kenntnisse anschaulich zu vermitteln.

